![]() Fusion – solide à liquide
Fusion – solide à liquide ![]() Point de fusion des substances pures et impures
Point de fusion des substances pures et impures
![]() Congélation – liquide à solide
Congélation – liquide à solide ![]() Points de fusion
Points de fusion
 La fusion et la congélation font référence aux changements d’état qui se produisent lorsque les états solide et liquide s’échangent. La fusion se produit lorsqu’un solide est chauffé et se transforme en liquide et la congélation se produit lorsqu’un liquide est refroidi et se transforme en solide.
La fusion et la congélation font référence aux changements d’état qui se produisent lorsque les états solide et liquide s’échangent. La fusion se produit lorsqu’un solide est chauffé et se transforme en liquide et la congélation se produit lorsqu’un liquide est refroidi et se transforme en solide.
Fusion – solide en liquide
Lorsqu’un solide est chauffé, ses particules gagnent suffisamment d’énergie pour surmonter les forces de liaison les maintenant fermement en place. Ils commencent à se déplacer, mais restent proches de leurs particules voisines, roulant les unes autour des autres. Ce mouvement de particules permet à la substance de s’écouler et de former un liquide. Les solides et les liquides ont une densité similaire, c’est-à-dire un nombre de particules par unité de volume. Ils ne diffèrent que par la capacité du liquide à s’écouler et à changer de forme pour occuper la forme de la partie inférieure de son récipient.
 |
Particules pendant la fusion |
Point de fusion des substances pures et impures
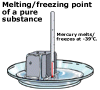 Pour les substances pures, la température à laquelle la fusion et la congélation se produisent est assez nette et s’appelle le point de fusion de la substance. Pour les substances impures, la fusion et la congélation se produisent plus progressivement sur une plage de température. C’est une façon pour les chimistes d’identifier la pureté d’une substance; une substance pure fondra à une température définie tandis que plus une substance est impure, plus son point de fusion variera sur une plage de températures.
Pour les substances pures, la température à laquelle la fusion et la congélation se produisent est assez nette et s’appelle le point de fusion de la substance. Pour les substances impures, la fusion et la congélation se produisent plus progressivement sur une plage de température. C’est une façon pour les chimistes d’identifier la pureté d’une substance; une substance pure fondra à une température définie tandis que plus une substance est impure, plus son point de fusion variera sur une plage de températures.
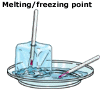 Congélation – liquide à solide
Congélation – liquide à solide
La congélation se produit lorsqu’un liquide est refroidi et se transforme en solide. Lors du refroidissement, les particules dans un liquide perdent de l’énergie, cessent de se déplacer et se déposent dans un arrangement stable, formant un solide. La congélation se produit à la même température que la fusion, par conséquent, le point de fusion et le point de congélation d’une substance sont à la même température. Le point de fusion/ congélation d’une substance est défini comme la température au-dessus de laquelle la substance est liquide et en dessous de laquelle elle est solide.
 |
Gel |
Points de fusion
Différents solides ont des points de fusion différents en fonction de la force de liaison entre les particules et de la masse des particules. Essentiellement, plus les particules dans le solide sont lourdes et plus la liaison est forte, plus le point de fusion est élevé.
L’hélium, la substance liée la plus légère et la plus faible connue, a un point de fusion très proche du zéro absolu, soit – 273°C. À l’autre extrémité de l’échelle, le tungstène, constitué de particules beaucoup plus lourdes à très forte liaison, fond à 3410°C
| Copyright propriété de l’État de Victoria (Department of Education and Early Childhood Development). Utilisé avec permission. |